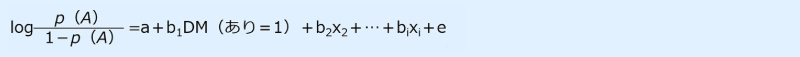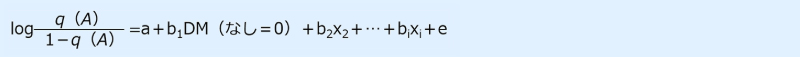提供元:CareNet.com

本連載は、臨床研究のノウハウを身につけたいけれど、メンター不在の臨床現場で悩める医療者のための、「実践的」臨床研究入門講座です。臨床研究の実践や論文執筆に必要な臨床疫学や生物統計の基本について、架空の臨床シナリオに基づいた仮想データ・セットや、実際に英語論文化した臨床研究の実例を用いて、解説していきます。
ロジスティック回帰モデルによる交絡因子調整の実際
前回までロジスティック回帰モデルの基本的な考え方を説明しました。今回は実際に仮想データ・セットを用いて、EZR(Easy R)を使用したロジスティック回帰モデルによる交絡因子の調整方法について解説します。
はじめに、以下の手順で仮想データ・セットをEZRにインポートします。
「ファイル」→「データのインポート」→「Excelのデータをインポート」
次にメニューバーから
「統計解析」→「名義変数の解析」→「二値変数に対する多変量解析(ロジスティック回帰)」
を選択すると、下図のポップアップウィンドウが開きます。
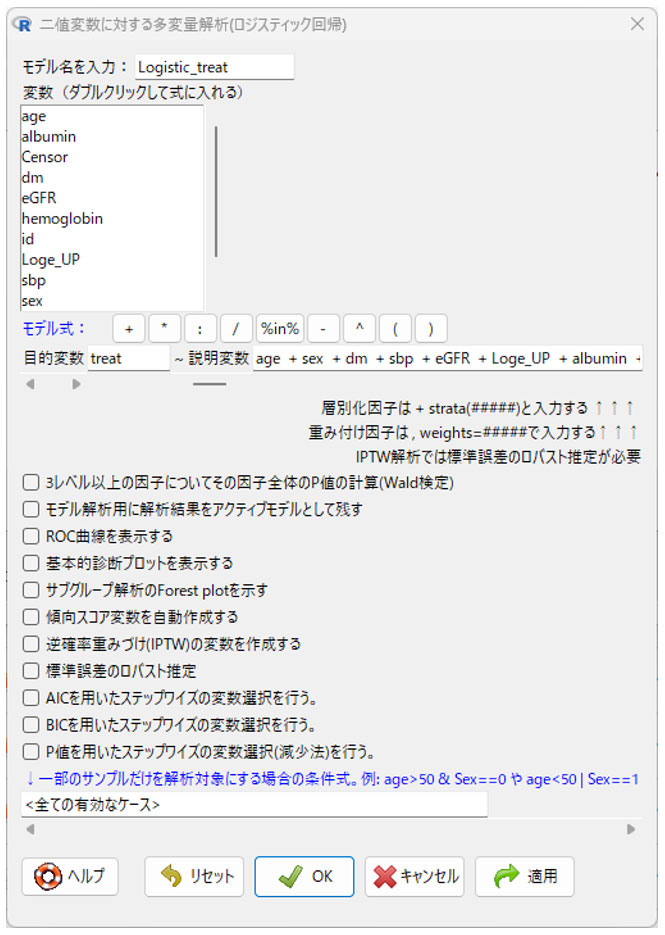
モデル名には「Logistic_treat」などと入力
モデル式は以下のように選択します(連載第60回参照)。
目的変数(左辺):treat(厳格低たんぱく食の遵守の有無)
説明変数(右辺):下記のtreat以外のすべての説明変数(交絡因子)を「+」でつないで選択
・age(年齢)、sex(性別)、dm(糖尿病の有無)、sbp(血圧)、eGFR(ベースラインeGFR)、Loge_UP(蛋白尿定量_対数変換)、albumin(血清アルブミン値)、hemoglobin(ヘモグロビン値)
・age+sex+dm+sbp+eGFR+Loge_UP+albumin+hemoglobin
「OK」をクリックすると、EZRのRコマンダー出力ウィンドウに下記のコードが表示されます。
Logistic_treat <- glm(treat ~ age + sex + dm + sbp + eGFR + Loge_UP + albumin + hemoglobin , family=binomial(logit), data=Dataset)
「Dataset」というデータを使用し、2値のカテゴリ変数である「treat」を目的変数として、~以下の8つの説明変数(交絡因子)で説明するロジスティック回帰分析(binomial(logit))を実行し、その計算結果を「Logistic_treat」というモデル名で保存
多変量ロジスティック回帰分析の結果は出力ウィンドウの最後に表示されており、説明変数ごとの調整オッズ比(odds ratio:OR)と95%信頼区間(95% confidence interval:95%CI)およびp値が示されています(下図)。ちなみにこの出力結果のp値の表記法は科学的記数法と言われるもので、たとえば”e-04″は10の-4乗(0.0001)を表しています。したがってageのp値は、1.25×0.0001=0.000125となり有意水準0.05を下回っています。
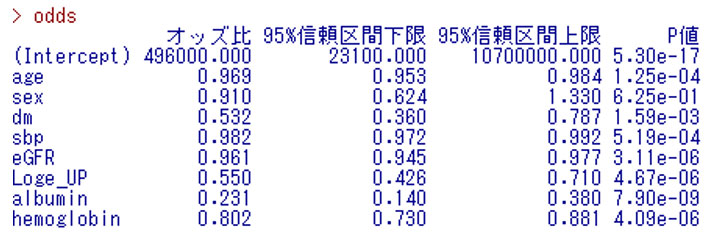
この表の結果の臨床的解釈を以下のように考えてみました。
・age(年齢):調整OR 0.969(95%CI:0.953~0.984)
・年齢が1歳増えるごとにtreat=1(厳格低たんぱく食の遵守あり)のORが3.1%(1-0.969)低下。
・高齢になるほど、低栄養などの懸念から厳格低たんぱく食の導入・継続は慎重となる可能性があります。
・dm(糖尿病の有無):調整OR 0.532(95%CI:0.360~0.787)
・糖尿病あり(dm=1)はなし(dm=0)に比べて、treat=1のORが47%(1-0.532)低い。
・糖尿病併発例では非糖尿病例と比べて、厳格低たんぱく食の導入・継続が困難である可能性が示唆されます。
・sbp(血圧):調整OR 0.982(95%CI:0.972~0.992)
・血圧が1mmHg高いほどtreat=1のORが1.8%(1-0.982)低い。
※変化幅を10倍(10mmHg)にしたほうがイメージしやすいかもしれません。その場合は推定値を10乗(0.98210≒0.834)します。
・血圧が10mmHg高いほどtreat=1のORが16.6%(1-0.834)低い。
・血圧管理の悪い例では、厳格低たんぱく食の導入・継続が困難な可能性が考えられます。
・eGFR(ベースラインeGFR):調整OR 0.961(95%CI:0.945~0.977)
・eGFRが1単位高いごとに、treat=1のORが約3.9%(1-0.961)低下。
・腎機能低下が進むほど、厳格低たんぱく食の導入・継続がなされている可能性があります。
・Loge_UP(蛋白尿定量_対数変換):OR 0.550(95%CI:0.426~0.710)
・蛋白尿が増えると(自然対数e倍)、treat=1のORが45%(1-0.550)低下。
・蛋白尿が多い例ほど、厳格低たんぱく食の導入・継続がなされている可能性があります。
※なお、ネフローゼ症候群は今回の研究対象からは除外されています(連載第40回参照)。
・albumin(血清アルブミン値):OR 0.231(95%CI:0.140~0.380)
・hemoglobin(ヘモグロビン値):OR 0.802(95%CI:0.730~0.881)
・ 血清アルブミン値が1単位(g/dL)、ヘモグロビン値が1単位(g/dL)増加するごとに、treat=1のORがそれぞれ76.9%(1-0.231)、19.8%(1-0.802)低下。
・血清アルブミン値が低いほど、ヘモグロビン値が低いほど、厳格低たんぱく食の導入・継続がなされているという結果ですが、横断的なベースラインデータの解析であり、逆因果の可能性に注意が必要です。
講師紹介

長谷川 毅 ( はせがわ たけし ) 氏
昭和医科大学臨床疫学研究所 所長・教授
昭和医科大学大学院医学研究科 衛生学・公衆衛生学分野/腎臓内科学分野 兼担教授
福島県立医科大学臨床研究イノベーションセンター 特任教授
[略歴]
1996年昭和大学(現昭和医科大学)医学部卒業。
2007年京都大学大学院医学研究科臨床情報疫学分野(臨床研究者養成コース)修了。
都市型および地方型の地域中核病院で一般内科から腎臓内科専門診療、三次救急から亜急性期リハビリテーション診療まで臨床経験を積む。その臨床経験の中で生じた「臨床上の疑問」を科学的に可視化したいという思いが募り、京都の公衆衛生大学院で臨床疫学を学び、米国留学を経て現在に至る。
バックナンバー
39. リサーチ・クエスチョンのブラッシュアップ‐E(要因)およびC(比較対照)設定の要点と実際 その2
38. リサーチ・クエスチョンのブラッシュアップ‐E(要因)およびC(比較対照)設定の要点と実際 その1
37. リサーチ・クエスチョンのブラッシュアップ‐O(アウトカム)設定の要点と実際 その2
36. リサーチ・クエスチョンのブラッシュアップ‐O(アウトカム)設定の要点と実際 その1
35. リサーチ・クエスチョンのブラッシュアップーP(対象)設定の要点と実際 その2
34. リサーチ・クエスチョンのブラッシュアップーP(対象)設定の要点と実際 その1
33. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その8
32. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その7
31. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その6
30. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その5
29. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その4
28. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その3
27. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その2
26. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 実際にPubMed検索式を作ってみる その1
25. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 PubMed検索 その5
24. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 PubMed検索 その4
23. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 PubMed検索 その3
22. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 PubMed検索 その2
21. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 1次情報源の活用 PubMed検索 その1
20. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 学術誌、論文、著者の影響力の指標 その3
19. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 学術誌、論文、著者の影響力の指標 その2
18. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 学術誌、論文、著者の影響力の指標 その1
17. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー CONNECTED PAPERSの活用 その3
16.リサーチ・クエスチョンのブラッシュアップー関連研究レビュー CONNECTED PAPERSの活用 その2
15. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー CONNECTED PAPERSの活用 その1
14. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー コクラン・ライブラリーの活用 その3
13. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー コクラン・ライブラリーの活用 その2
12. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー コクラン・ライブラリーの活用その1
11. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー UpToDateの活用その2
10. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー UpToDateの活用その1
9. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 文献管理その3
8. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 文献管理その2
7. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 文献管理その1
6. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 診療ガイドラインの活用その3
5. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 診療ガイドラインの活用その2
4. リサーチ・クエスチョンのブラッシュアップー関連研究レビュー 診療ガイドラインの活用その1
3. リサーチ・クエスチョンのブラッシュアップー関連研究レビューその2
掲載内容はケアネットの見解を述べるものではございません。
(すべての写真・図表等の無断転載を禁じます。)